Acid hexafluorosilicic
Problema Acid hexafluorosilicic este un subiect care a generat mare interes și controversă în ultima vreme. Cu abordări și perspective diferite, Acid hexafluorosilicic a fost subiect de dezbatere și cercetare în diferite domenii ale cunoașterii. De la impactul său asupra societății până la implicațiile sale la nivel individual, Acid hexafluorosilicic a captat atenția academicilor, specialiștilor și oamenilor obișnuiți. În acest articol, vom explora diferite aspecte legate de Acid hexafluorosilicic, analizând relevanța acestuia și dezvăluind posibilele sale consecințe. În plus, vom examina modul în care Acid hexafluorosilicic a modelat și va continua să modeleze peisajul actual, oferind o vedere cuprinzătoare a acestui subiect important.
| Acid hexafluorosilicic | |
 | |
 | |
| Identificare | |
|---|---|
| Număr CAS | 16961-83-4 |
| PubChem CID | 21863527 |
| Informații generale | |
| Formulă chimică | F6H2Si |
| Masă molară | 144,09 g/mol |
| Proprietăți | |
| Densitate | 1,22 g/cm3 (25% sol.) |
| Punct de topire | < −30 °C (35% sol.) |
| Punct de fierbere | 108,5 °C, desc. |
| Pericol | |
| Fraze R | R34, R25 |
| Fraze S | (S1/2), S26, S27, S45 |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acidul hexafluorosilicic este un compus anorganic cu formula H2SiF6 sau (H
3O)
2SiF
6 (pentru forma hidratată, de asemenea scrisă și (H
3O)
2). Este un lichid incolor, mai rar întâlnit în formă concentrată. Are un miros înțepător și este produs în natură în vulcani.[1][2] Sărurile acestui acid se numesc hexafluorosilicați.
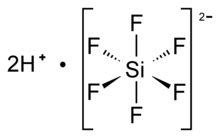
Structură
Referințe
- ^ Palache, C., Berman, H., and Frondel, C. (1951) Dana’s System of Mineralogy, Volume II: Halides, Nitrates, Borates, Carbonates, Sulfates, Phosphates, Arsenates, Tungstates, Molybdates, etc. John Wiley and Sons, Inc., New York, 7th edition.
- ^ Anthony, J.W., Bideaux, R.A., Bladh, K.W., and Nichols, M.C. (1997) Handbook of Mineralogy, Volume III: Halides, Hydroxides, Oxides. Mineral Data Publishing, Tucson.
- date despre bararit Arhivat în , la Wayback Machine.
- date despre cryptohalit Arhivat în , la Wayback Machine.

