Clorură de sodiu
În acest articol, vom explora lumea fascinantă a lui Clorură de sodiu și toate implicațiile pe care le are asupra societății noastre actuale. De la impactul său asupra culturii populare până la relevanța sa în viața de zi cu zi, Clorură de sodiu a jucat un rol crucial în diferite domenii ale vieții noastre. În plus, vom examina evoluția lui Clorură de sodiu în timp și modul în care ne-a influențat percepțiile și acțiunile. Printr-o analiză cuprinzătoare, vom dezvălui misterele și complexitățile din jurul lui Clorură de sodiu, oferind o perspectivă profundă și perspicace asupra acestui subiect de relevanță universală.
| Clorură de sodiu | |
 Cristale de sare marină | |
 Structura cristalină | |
| Denumiri | |
|---|---|
| Alte denumiri | Clorură de natriu, sare de bucătărie, halit, sare gemă, aurul alb |
| Identificare | |
| Număr CAS | 7647-14-5 |
| ChEMBL | CHEMBL1200574 |
| PubChem CID | 5234 |
| Informații generale | |
| Formulă chimică | NaCl |
| Aspect | masă solidă, cristalizată, de culoare albă, higroscopică |
| Masă molară | 58,44 g/mol |
| Proprietăți | |
| Densitate | 2,165 g/cm−3 |
| Starea de agregare | solidă |
| Punct de topire | 801 °C, 1074 K, 1474 °F |
| Punct de fierbere | 1413 °C, 1686 K, 2575 °F |
| Solubilitate | foarte bună în apă (359 g L−1), în amoniac (21,5 g L−1) și în metanol (14,9 g L−1) |
| Structură cristalină | cristale cubice |
| Anion | clor |
| Cation | sodiu |
| Duritate (Scara Mohs) | 2 1/2 |
| Indice de refracție(nD) | 1,544202 |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Clorura de sodiu (denumită impropriu și sare de bucătărie) este sarea sodiului cu acidul clorhidric și are formula NaCl. Clorura de sodiu se obține prin reacția dintre acidul clorhidric și hidroxidul de sodiu.
Proprietăți fizice
Este o substanță solidă, ionică, cristalină (structură cubică cu fețe centrate); punctul de fierbere este 1413°C iar punctul de topire 801°C. Este solubilă în apă - 359 g/l la 20°C și 391 la 100°C . Sarea este higroscopică.
Densitatea sării este 2,165 g/cm3 (toate datele se referă la sarea pură). Duritatea sa este de 2,5 pe scara Mohs, adică între gips și calcit.
Rezistența la compresiune variază în funcție de încărcarea probei, formă, structură cristalină, stratificații etc. Din probele executate se constată[necesită citare]:
- Limita de elasticitate (sarcina, în kgf/cm2, până la care sarea se comportă ca un material elastic) este de 15–25 kgf/cm2.
- Limita deformațiilor plastice de la 25 la 100 kg/cm2: sarea se comportă ca un material plastic, dar deformațiile sunt foarte mici. Această zonă se numește regim al deformațiilor plastice mici.
- Limitele deformațiilor plastice mari cuprinse între 100kgf/cm2 și ruperea probei.
Rezistențe mecanice, tracțiunea, forfecarea și încărcarea arată valori foarte variate pentru calitatea sării. Astfel, pentru rezistența la tracțiune, valoarea medie este de 18 kgf/cm2 — cu 9,4 pentru sarea albă, 16,2 pentru cea vărgată și 28,5 pentru cea vânătă.
Densitatea soluțiilor apoase
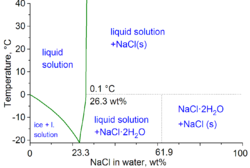
| NaCl, wt% | Teq, °C | ρ, g/cm3 | n | η, mPa·s |
|---|---|---|---|---|
| 0 | 0 | 1.002 | ||
| 0.5 | −0.3 | 1.0018 | 1.3339 | 1.011 |
| 1 | −0.59 | 1.0053 | 1.3347 | 1.02 |
| 2 | −1.19 | 1.0125 | 1.3365 | 1.036 |
| 3 | −1.79 | 1.0196 | 1.3383 | 1.052 |
| 4 | −2.41 | 1.0268 | 1.34 | 1.068 |
| 5 | −3.05 | 1.034 | 1.3418 | 1.085 |
| 6 | −3.7 | 1.0413 | 1.3435 | 1.104 |
| 7 | −4.38 | 1.0486 | 1.3453 | 1.124 |
| 8 | −5.08 | 1.0559 | 1.347 | 1.145 |
| 9 | −5.81 | 1.0633 | 1.3488 | 1.168 |
| 10 | −6.56 | 1.0707 | 1.3505 | 1.193 |
| 12 | −8.18 | 1.0857 | 1.3541 | 1.25 |
| 14 | −9.94 | 1.1008 | 1.3576 | 1.317 |
| 16 | −11.89 | 1.1162 | 1.3612 | 1.388 |
| 18 | −14.04 | 1.1319 | 1.3648 | 1.463 |
| 20 | −16.46 | 1.1478 | 1.3684 | 1.557 |
| 22 | −19.18 | 1.164 | 1.3721 | 1.676 |
| 23.3 | −21.1 | |||
| 23.7 | −17.3 | |||
| 24.9 | −11.1 | |||
| 26.1 | −2.7 | |||
| 26.28 | 0 | |||
| 26.32 | 10 | |||
| 26.41 | 20 | |||
| 26.45 | 25 | |||
| 26.52 | 30 | |||
| 26.67 | 40 | |||
| 26.84 | 50 | |||
| 27.03 | 60 | |||
| 27.25 | 70 | |||
| 27.5 | 80 | |||
| 27.78 | 90 | |||
| 28.05 | 100 |
Notă: ρ e densitatea, n e indice de refracție la 589 nm, η e viscositatea, toate la 20 °C; Teq e temperatura de echilibru între două faze: gheață/soluție lichidă pentru Teq < 0–0.1 °C și NaCl/soluție lichidă pentru Teq above 0.1 °C.
Electroliza
Electroliza soluției
Electroliza unei soluții de clorură de sodiu (soluție denumită și saramură) este un procedeu foarte folositor în industrie, deoarece, în urma acestei reacții se obține soda caustică, după reacția:
- 2 NaCl + 2 H2O → 2 NaOH + H2 + Cl2
În România, astfel s-a produs sodă caustică.
Electroliza topiturii
Făcându-se electroliza unei topituri, se pot obține elementele chimice din care este compusă sarea de bucătărie: sodiu și clor.
- 2 NaCl → 2 Na + Cl2
Referințe
- ^ „Clorură de sodiu”, sodium chloride (în engleză), PubChem, accesat în
- ^ Format:RubberBible86th
Vezi și
Legături externe
![]() Materiale media legate de Clorură de sodiu la Wikimedia Commons
Materiale media legate de Clorură de sodiu la Wikimedia Commons
- Sarea, Timpul și Omul Arhivat în , la Wayback Machine.
- Exploatarea sării în Dacia romană
- Exploatarea sării în spațiul carpato-dunărean în perioada post-romană și cea a marilor migrații
- Exploatarea tradițională a sării în Transilvania
- Densitatea soluțiilor de sare
