Hidrazonă
În acest articol, vom explora subiectul Hidrazonă în profunzime. De la rădăcinile sale istorice până la relevanța sa astăzi, acest subiect este de cea mai mare importanță și merită să fie analizat în detaliu. Pe parcursul următoarelor rânduri, vom examina diferitele aspecte care alcătuiesc Hidrazonă, precum și impactul acestuia asupra diferitelor zone ale societății. Prin cercetare și analiză critică, sperăm să facem lumină asupra acestui subiect și să oferim cititorilor noștri o înțelegere mai profundă și mai completă a Hidrazonă.
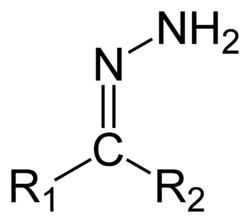
Hidrazonele reprezintă o clasă de compuși organici cu structura generală R
1R
2C=NNH
2.[1] Sunt asemănătoare cu cetonele și aldehidele, în structura cărora se înlocuiește atomul de oxigen cu o grupă funcțională NNH
2.
Obținere
Hidrazonele se pot obține prin reacția dintre hidrazină și o cetonă sau o aldehidă:[2][3]
Fenilhidrazina reacționează cu zaharurile reducătoare pentru a forma hidrazone, cunoscute sub numele specific de osazone; formarea lor a fost dezvoltată de către chimistul german Emil Fischer, ca test pentru a diferenția monozaharidele.[4][5]
Proprietăți
Hidrazonele sunt sensibile la reacții de hidroliză:
- R2C=N−NR'2 + H2O → R2C=O + H2N−NR'2
Alchilhidrazonele sunt de 102 până la 103 ori mai sensibile la hidroliză decât oximele analoge.[6]
Hidrazonele acționează ca intermediari în reacțiile de reducere Wolff-Kishner, care este un proces de reducere a compușilor carbonilici la alcani:[7]

Gallery
- Exemple de hidrazone
-
Hidrazona benzofenonei[8]
-
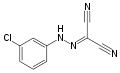
Hidrazona m-clorofenil carbonil cianurii
-
Giromitrină, o toxină
-
Dihidralazină, un medicament antihipertensiv
-
Furazolidonă, un medicament antiinfecțios
Vezi și
Referințe
- ^ March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ed.), New York: Wiley, ISBN 0-471-85472-7
- ^ Stork, G.; Benaim, J. (), „Monoalkylation of α,β-Unsaturated Ketones via Metalloenamines: 1-butyl-10-methyl-Δ1(9)-2-octalone”, Org. Synth., 57: 69; Collective Volume, 6, p. 242
- ^ Day, A. C.; Whiting, M. C. (), „Acetone hydrazone”, Org. Synth., 50: 3; Collective Volume, 6, p. 10
- ^ Fischer, Emil (). „Schmelzpunkt des Phenylhydrazins und einiger Osazone”. Berichte der Deutschen Chemischen Gesellschaft. 41: 73–77. doi:10.1002/cber.19080410120.
- ^ Fischer, Emil (). „Ueber einige Osazone und Hydrazone der Zuckergruppe”. Berichte der Deutschen Chemischen Gesellschaft. 27 (2): 2486–2492. doi:10.1002/cber.189402702249.
- ^ Kalia, J.; Raines, R. T. (). „Hydrolytic stability of hydrazones and oximes”. Angew. Chem. Int. Ed. 47 (39): 7523–6. doi:10.1002/anie.200802651. PMC 2743602
 . PMID 18712739.
. PMID 18712739.
- ^ Carey, Francis A.; Sundberg, Richard J. (). Advanced Organic Chemistry: Part B: Reactions and Synthesis (ed. 5th). New York: Springer. p. 453. ISBN 978-0387683546.
- ^ Tameem, Abdassalam Abdelhafiz; Salhin, Abdussalam; Saad, Bahruddin; Rahman, Ismail Ab.; Saleh, Muhammad Idiris; Ng, Shea-Lin; Fun, Hoong-Kun (). „Benzophenone 2,4-dinitrophenylhydrazone”. Acta Crystallographica Section E. 62 (12): o5686–o5688. doi:10.1107/S1600536806048112.